
GÉNÉRALITÉS
:
L'air est un mélange de gaz, principal constituant
de l'atmosphère terrestre.
Masse molaire théorique de l'air
sec (mais bien pratique !) : 28,965338
g·mol-1 (ou 28,966).
L'air qui nous environne et qui entoure la Terre, constitue une
partie de l'atmosphère appelée
troposphère ; cette couche
a une épaisseur variant de 17 km au dessus de
l'équateur à 7-8 km au-dessus des pôles.
Il est composé principalement d'environ 78 % en volume de
diazote
[N2= 78,08 %] et de 21 %
environ de dioxygène
[O2= 20,95 %], et d'environ
1 % d'autres gaz et de vapeur
d'eau (de 0 à 7,6% suivant la température).
Composition de l'air
sec (au niveau du sol)
:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Nota : les proportions massiques peuvent être
évaluées approximativement en multipliant les
proportions volumiques par le rapport de la masse molaire du gaz
considéré, divisé par la masse molaire
théorique de l'air soit 28,965338; par exemple dans le
cas du CO2 ce rapport n'est pas négligeable
puisqu'il vaut (44,0098/28,965338) = 1,5194,
d'ou la teneur massique en CO2 dans
l'air (2019) égale à environ
(411,50 x 1,5194) = 625,23 ppm
(ppmm), ou dans le cas de l'hydrogène
à 0.050 ppm en masse pour 0,72 ppm en volume.
-------------------
NOTES : le taux de dioxyde de carbone ( CO2 ) dans l'air varie avec le temps. Le taux moyen annuel augmente de 1,2 à 1,4 ppm (en volume, ou ppmv) par an. De l'ordre de 389 ppmv (0,0389 %) à mi-2010, il était de 278 ppmv à avant la révolution industrielle, de 315 ppmv en 1958, de 330 ppmv en 1974, de 353 ppmv en 1990, de 370 ppmv en 2000, de 405 ppmv en 2017/2018 et de 411,50 ppmv en 2019 (source NOAA, USA) :

Ce gaz à effet de serre
(GES)
joue un rôle important dans le réchauffement climatique
de la planète.
Le méthane est un
autre GES majeur dont le taux augmente avec le temps : 0,8 ppmv
à l'époque pré-industrielle, 1,585 ppmv en 1985,
1,663 ppmv en 1992, 1,676 ppmv en 1996, 1,800 ppmv en 2009 et 1,870
ppmv en 2019.
Nota : avant l’ère industrielle, les niveaux mondiaux de
méthane étaient faibles et relativement stables depuis
800.000 années, allant de 300 à 800 ppb (parties par
millirad);
avec l’avènement de l’agriculture, puis de
l’exploitation des combustibles fossiles, les niveaux de
méthane ont grimpé en flèche pour atteindre donc
maintenant plus de 1 800 ppb.).
La proportion de vapeur d'eau
dépend du taux d'hygrométrie
(degré d'humidité) de l'air et
de sa température. Elle est limitée par la pression de
vapeur saturante de l'eau.
NB: la vapeur d'eau dans l'air fluctue entre 0,4 % et 4 %, et en est
le principal gaz à effet de serre.
Diagramme enthalpique de l'air humide (Carrier) :
Nota : toutes ces grandeurs ne sont pas indépendantes. Connaître deux grandeurs permet de calculer toutes les autres.
A l'état gazeux, l'eau ne modifie pas la transparence de
l'air mais condensée en fines gouttelettes ou
solidifiée en cristaux de glace, l'atmosphère devient
alors opaque. Les masses nuageuses (lien
interne sur les nuages) sont la manifestation directe de la
présence d'eau dans l'atmosphère.
Par ailleurs, la pression
varie avec l'altitude :
%3Df(H).jpg)
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
||||
|
|
|
|
||||
|
|
|
|


Nota : la pression atmosphérique diminue donc avec
l'altitude : elle diminue, exponentiellement, d'un facteur 10 chaque
fois que l'on s'élève de 16 km : il est donc possible
d'utiliser la pression pour mesurer la hauteur, ce qui est le
principe de base de l'altimètre utilisé en
aéronautique (également il y a
variation avec la latitude/longitude terrestre).
Formule approché de l'Organisation de l'Aviation Civile
Internationale (OACI) : pression en altitude =
f[pression au sol (Psol en hpa) et
altitude (alti en m)]
(valable pour la troposphère qui
s'étend de 0 à 11 km, et ne prend pas en compte la
vapeur d'eau)

PROPRIETES.
L'air étant un gaz compressible, sa masse volumique
est fonction de la pression, de la température et du taux
d'humidité.
Pour de l'air sec sous pression atmosphérique
"normale", soit 1013,25 hPa, on prend généralement
Mv = 1,293 kg m3-1 à
0°C et 1,205 à 20°C :
air.jpg)
Estimation de la masse volumique de
l'air
sec en fonction de la
température (P = 1 atm =
1 013,25 hPa) :
Pour l'air sec
et humide >>>
téléchargement du programme
MVP-air.exe
(zip auto-extractible, feuille tableur 127 ko [343 ko
dézippé]),
et lien
externe.
Vitesse du son dans l'air.
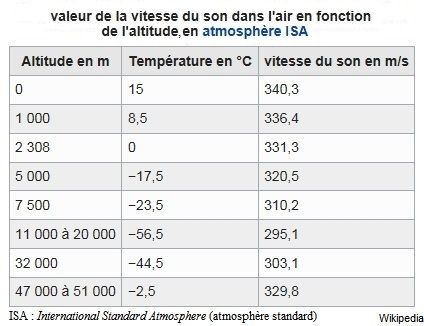
La masse molaire théorique est d'environ 28,965 g
mol-1.
L'air gazeux commence
à se liquéfier
à -194,5 °C (78,65
K) pour P = 1 atm.
(début de l'ébullition de
l'air
liquide à -194,3
°C (78,85
K) pour P = 1 atm).
Début de solidification de l'air
liquide : -216,2
(56,95
K), pour P = 1 atm.
(la fusion de l'air solide (air
congelé) commence
à -213,4 °C (59,75
K), pour P = 1 atm).
Point critique :
Il est disponible sous forme de gaz comprimé ou de liquide. Il est ininflammable.
Quelques
caractéristiques
:
Principales applications
industrielles.
L'oxydation directe de l'éthylène ou du
propylène par l'air ou l'air enrichi en oxygène en
présence d'un catalyseur produit l'oxyde
d'éthylène ou de propylène.
Laboratoires.
L'air est utilisé pour calibrer les analyseurs
d'impuretés en trace, les analyseurs de contrôle de
l'environnement ou les analyseurs de contrôle des
atmosphères de travail. L'air est aussi utilisé
comme gaz de dilution pour un certain nombre de mélanges de
calibration.
L'air est utilisé comme gaz de combustion dans des
détecteurs de chromatographes en phase gazeuse (Ionisation
de flamme ou FID, Photomètrie de fliamme ou FPD) et dans
les spectrophotomètres par absorption atomique.
Pétrole et dérivés.
L'air ou l'air enrichi en oxygène est utilisé comme
agent oxydant dans le procédé Clauss de combustion
du soufre en dioxide de soufre.
Divers.
Téléchargement des Fiches Techniques de
Sécurité -
Air Liquide
(fichiers
pdf) : Air
comprimé et
Air
liquide.