GÉNÉRALITÉS
:
Après l'hydrogène,
l'hélium est l'élément le plus abondant
de l'Univers. Il est présent à 25% en masse dans le
Soleil (et des planètes Jupiter et
Saturne), et dans la plupart des étoiles.
C'est est un des gaz de l'air atmosphèrique
(voir ce
lien sur l'air), et il
représente 0,00052% (5,2
ppmv) du volume total de l'atmosphère
terrestre.
Il appartient au groupe des gaz "rares" (parfois
appelé "gaz nobles"), avec l’argon,
le néon, le krypton
et le xénon.
De formule He, c'est un gaz neutre et incolore comme
l'azote N2,
à l'état naturel, sur Terre il est présent dans
l'air et on peut également le trouver sous forme fossile dans
le sous-sol, dans des poches de gaz naturel de quelques gisements
pétroliers dans certaines régions des USA,
d'Algérie et de Pologne. On l'extrait alors au moyen de
forages profonds.
Masse atomique : 4,0026
g mol-1
(numéro atomique Z = 2).
Isotopes : 3He, 4He et 5He,
6He, 7He et 8He, dont 2 stables >
4He
(99,999863 % sur Terre ) et
3He (0,000137
%) aux propriétés assez différentes.
Propriétés de l'hélium
L'hélium est un un gaz incolore, inodore,
pratiquement inerte et ininflammable.
Il est surtout extrait du gaz naturel (qui peut en
contenir jusqu'à 7 %), par distillation
fractionnée.
C'est est un gaz extrêmement léger et il est par
conséquent très volatile.
Très faiblement soluble dans l'eau : 0,0089 vol/vol
(8,9 ml dans 1 litre d'eau,
à 20 °C et
sous 1 bar), donc le moins soluble des gaz
connus.
Avec le néon,
l'hélium est chimiquement le moins réactif de tous les
corps dans les conditions normales, en raison de sa valence
égale à 0.
Comme les autres gaz "nobles", l'hélium a des niveaux
d'énergie métastables qui lui permettent de rester
excité dans une décharge électrique dont la
tension est inférieure à son potentiel d'ionisation.
Ceci permet son utilisation dans les lampes à
décharge.
Aux conditions "normales" de pression (1013,25
hPa), c'est un gaz beaucoup plus léger que l'air
(masse volumique) : 0,169
kg/m3 à 15 °C et 0,178 à
20°C.
Une fois refroidi en dessous de la température de -233,15
°C (40 K, température d'inversion de
Joule-Thomson ), l'hélium peut être
liquéfié seulement par le refroidissement dû
seulement à sa détente.
Il se liquéfie vers -269°C
(4,15 K) sous 1,013 bar (1
atm). Son point d'ébullition est par ailleurs, le plus
bas parmi les corps connus.
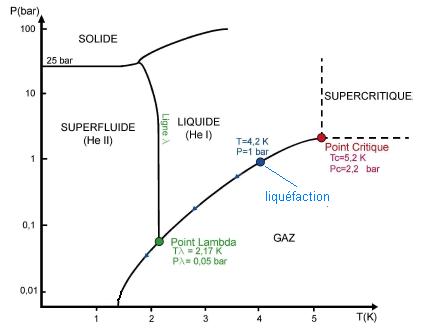
Nota : l’originalité de l’hélium vient du
fait qu’il possède deux phases liquides: une phase
liquide normale (He I) et une phase liquide superfluide (He II).
L’hélium ne possède donc pas de point triple mais
un point dit l
("lambda") à
l’intersection des phases gazeuse, liquide et
superfluide (quatrième phase).
Le Point l
se situe à T = -270,98 °C (2,17 K)
et Pression = 50 hPa (0,05 bar), et en dessous
de ce point se trouve l'état
superfluide qui est caractérisé par une
absence totale de viscosité, entre autres
propriétés remarquables (voir ce
lien et/ou celui-ci).
Le point de fusion de l'hélium solide
(hélium congelé) est à
-272,2 °C (0,95 K) sous 26
atmosphères, et c'est donc aussi le point approché, de
solidification de l'hélium
liquide.
Il reste liquide jusqu'au zéro absolu à des pressions
inférieures à 25 atm, il n'existe donc sous forme
solide qu'au-dessus d'une pression de 25 atm.
Point Critiques : Pression Pc = 0,227
MPa (2,27 bar) et
Température Tc = -268 °C
[5,15 K].

Quelques caractéristiques :
Utilisations.
Divers.
Comme l'hélium est plus léger que l'air, il peut
être utilisé pour gonfler des dirigeables et des ballons
libres ou captifs. Bien que l'hydrogène ait une force portante
approximativement 7 % supérieure, l'hélium a l'avantage
d'être incombustible (et même
ignifuge).
Le réservoir d'oxygène de la nouvelle
génération de lanceurs Ariane 5 est pressurisé
par un sous-système d'hélium liquide.
Effet sur l'homme.
La voix d'un individu qui a inhalé de l'hélium change
temporairement de timbre vers les harmoniques
élevés.
Risque de suffocation : une inhalation d’une grande
quantité comporte des risques d’asphyxie par privation
d’oxygène.
Lien
(canadien) sur les dangers des liquides cryogéniques.
A noter que l’atmosphère de la planète
Vénus contient 12 ppmv d’hélium (Terre : 5,2
ppmv).